Nel settore farmaceutico, l’aspetto regolatorio è sempre stato un elemento centrale. Garantire sicurezza, efficacia e qualità è una condizione imprescindibile, e il quadro normativo ha storicamente svolto questa funzione.
Nel 2026, tuttavia, il regolatorio non può più essere considerato un livello esterno rispetto all’innovazione. Non interviene a valle per valutare ciò che è stato sviluppato, ma contribuisce a definirne i confini fin dalle fasi iniziali.
Questo cambia il suo ruolo.
Innovazione più veloce, regole sotto pressione
Negli ultimi anni, il ritmo dell’innovazione è aumentato in modo significativo. Tecnologie come l’intelligenza artificiale, le piattaforme mRNA e i modelli di produzione avanzata introducono possibilità che non erano previste nei modelli regolatori tradizionali.
Il risultato è una tensione crescente: le regole devono adattarsi a contesti nuovi, ma non possono farlo con la stessa velocità delle tecnologie.
Questo scarto temporale è inevitabile, ma genera complessità per le aziende, che si trovano a operare in un quadro in evoluzione.
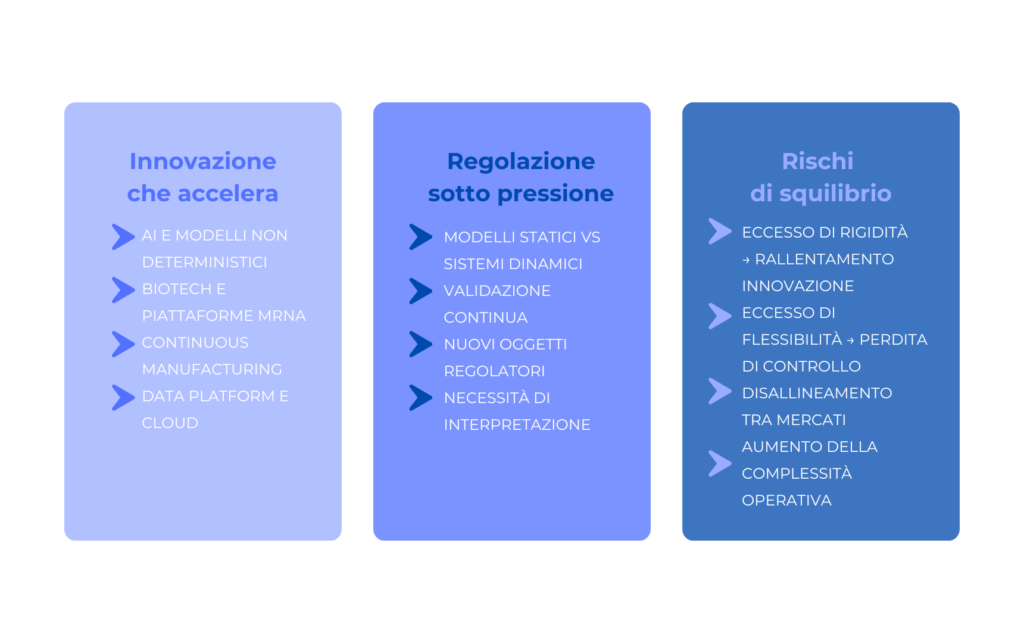
Il rischio di rallentare il sistema
Una regolamentazione troppo rigida può rallentare l’adozione dell’innovazione. Non perché ne impedisca lo sviluppo, ma perché ne rende più complessa l’implementazione.
Nel pharma, questo rischio è particolarmente rilevante. Il passaggio dalla ricerca all’utilizzo reale richiede approvazioni, validazioni e verifiche che possono allungare i tempi.
In alcuni casi, la difficoltà non è sviluppare una tecnologia, ma portarla sul mercato in modo conforme.
Il rischio opposto: perdere controllo
Allo stesso tempo, una regolamentazione troppo flessibile introduce un rischio opposto: perdita di controllo.
Nel pharma, questo non è un rischio teorico. La sicurezza dei pazienti e l’affidabilità dei prodotti non possono essere compromesse.
Il regolatorio deve quindi muoversi su un confine sottile, bilanciando apertura all’innovazione e mantenimento degli standard.
Nuovi oggetti regolatori
Un elemento di complessità riguarda la natura stessa delle tecnologie.
Un algoritmo, una piattaforma dati, un sistema basato su AI non sono oggetti facilmente assimilabili ai modelli tradizionali di valutazione. Non sono statici, evolvono nel tempo, dipendono dai dati.
Questo richiede nuovi approcci:
- valutazione del ciclo di vita
- monitoraggio continuo
- gestione del cambiamento
Il regolatorio si sposta da una logica statica a una dinamica.
Regolatorio dinamico: cosa sta cambiando davvero
Il modello regolatorio tradizionale nel pharma è stato costruito su sistemi stabili: prodotti definiti, processi controllati, risultati prevedibili.
Le nuove tecnologie stanno mettendo in discussione questo impianto.
Strumenti come intelligenza artificiale, piattaforme dati e processi produttivi avanzati introducono elementi dinamici, che evolvono nel tempo e richiedono un monitoraggio continuo.
La validazione non è più un evento, ma un processo.
In questo contesto, il regolatorio si sposta da una logica statica a una logica di ciclo di vita, in cui il controllo non si esaurisce nell’approvazione iniziale ma accompagna l’intero utilizzo del sistema.
👉 Il nodo non è aggiornare le regole, ma adattare il modo in cui vengono applicate.
Il ruolo dell’interpretazione
In questo contesto, la differenza non è solo nelle norme, ma nel modo in cui vengono interpretate.
Le aziende non possono limitarsi ad applicare regole esistenti. Devono sviluppare capacità interne di lettura del quadro regolatorio, anticipando evoluzioni e costruendo strategie coerenti.
Il regolatorio diventa così una competenza strategica, non solo una funzione di compliance.
Europa tra rigore e competitività
Il contesto europeo presenta caratteristiche specifiche. Da un lato, un elevato livello di protezione e attenzione alla sicurezza. Dall’altro, una crescente pressione competitiva da parte di altri mercati.
Il rischio è che un eccesso di complessità regolatoria possa ridurre la capacità di attrarre investimenti e innovazione. Allo stesso tempo, un allentamento indiscriminato potrebbe compromettere la fiducia nel sistema.
L’equilibrio è particolarmente delicato.
Regolatorio come leva, non solo vincolo
Una delle evoluzioni più interessanti riguarda la possibilità di utilizzare il regolatorio come leva per orientare lo sviluppo.
Linee guida, incentivi, percorsi accelerati: strumenti che non si limitano a controllare, ma contribuiscono a indirizzare l’innovazione.
In questo senso, il regolatorio non è solo un limite, ma un fattore attivo nel definire le traiettorie del settore.
Un sistema in evoluzione continua
Nel 2026, il quadro regolatorio del pharma è in continua evoluzione. Non esiste un punto di equilibrio stabile, ma un processo di adattamento costante.
Le aziende devono operare in questo contesto dinamico, sviluppando capacità di adattamento e integrazione tra funzioni.
Governare l’equilibrio
Il rapporto tra regolazione e innovazione non può essere risolto una volta per tutte. È un equilibrio da costruire e mantenere nel tempo.
Nel pharma, questo equilibrio non è solo tecnico o normativo. È industriale, economico e, in ultima analisi, sociale.
Ed è proprio nella capacità di governarlo che si gioca una parte rilevante del futuro del settore.